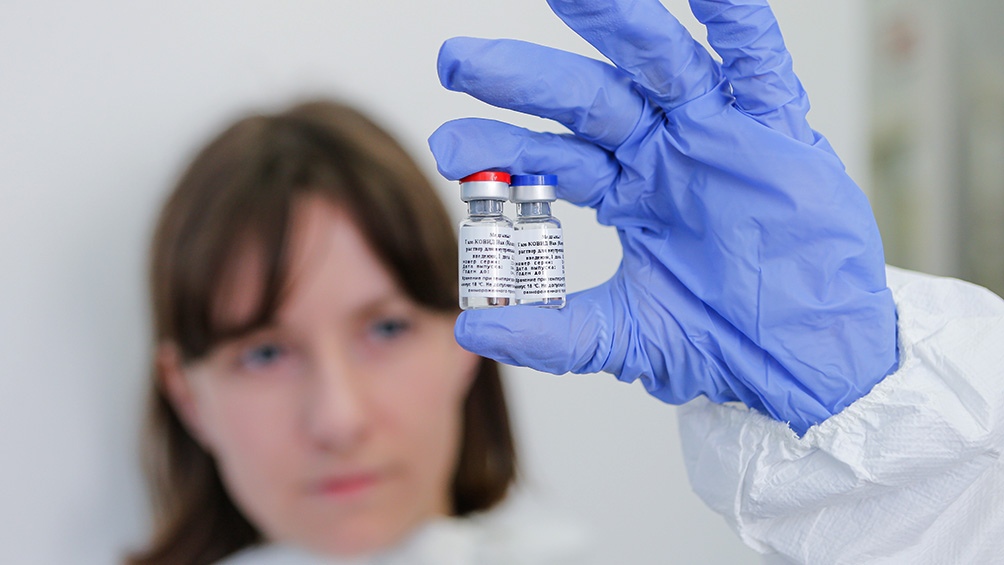
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) aprobó la utilización de la vacuna Sputnik V en personas con más de 60 años de edad, ya que «se encuentra en un margen aceptable la seguridad, inmunogenicidad y eficacia para el grupo etario», según comunicaron este martes desde el organismo.
La conclusión de la entidad gubernamental se dio a conocer «luego de analizada la nueva información aportada para la vacuna» proveniente de la Rusia.
De esta manera, «los datos de eficacia, inmunogenicidad y seguridad respecto a la población total del estudio con franja etaria 18 a 87 años reportaba un perfil de seguridad aceptable y no hubieron eventos adversos inesperados hasta el momento del análisis. Asimismo, considerando la cantidad de sujetos mayores de 60 años expuestos al producto en investigación, se sugirió un nuevo análisis de seguridad a la espera de eventos adversos que podrían observarse en un mayor número».
«En consecuencia, se recibió por parte del adquiriente, nueva documentación para su análisis, entre ellos el documento ’60 + Sinópsis del reporte clínico’ y el ‘Reporte de estudio clínico 04-Gam-COVID-Vac-2020 versión 2.0 del 15/01/2021’. Esta información reportó un rango de eficacia del 91,8% de la vacuna para mayores de 60 años; la inmunización de los voluntarios condujo a la formación de anticuerpos en el 98,1% el día 28 después de la vacunación y la variable de seguridad mostró un perfil que no difiere del observado en el resto de la población», detallaron desde ANMAT.
Asimismo, esta administración también aprobó el primer test rápido de detección de coronavirus que en aproximadamente 5 minutos y con una muestra de sangre permite conocer si una persona padeció o transita la enfermedad. Vale mencionar que iniciativas de este tipo ya existen pero habitualmente los componentes son importados desde Asia.
Desarrollado por un equipo de científicas y científicos de nuestro país, el diagnóstico «permitirá realizar estudios poblacionales a gran escala, mapeo y segregación de áreas. Podrá utilizarse, por ejemplo, en plazas, colectivos y escuelas para separar rápidamente a los positivos, a quienes luego se les podrá realizar un hisopado para aislar a los que están cursando actualmente la enfermedad», manifestaron desde el Instituto Nacional de Tecnología Industrial (INTI). «Teniendo en cuenta esta demanda, científicos del consorcio CINDEFI-Bamboo desarrollaron el primer test serológico rápido nacional, que mediante una gota de sangre permite saber si la persona está o estuvo en contacto con el virus SARS-CoV-2», ampliaron.
«Desde el consorcio se contactaron con nosotros porque necesitaban sustituir importaciones de un insumo conocido como IPTG (Isopropil-β-D-1-tiogalactopiranósido), para inducir la producción de la proteína N del coronavirus. Esta se coloca en las tiras reactivas del test y es clave, porque al ponerse en contacto con la sangre de la persona testeada, permite detectar la presencia de anticuerpos -en caso de tenerlos indicaría que el virus ingresó a su organismo-» explicó Laura Hermida, subgerente de Industria y Servicios de INTI.
Finalmente, Hermida asegura que «el desarrollo del insumo acompaña al proyecto en la sustitución de importaciones, clave para que el test pueda tener un precio accesible» y «a futuro, está previsto transferir la tecnología de producción para que una empresa nacional pueda fabricarlo».